Pertanyaan
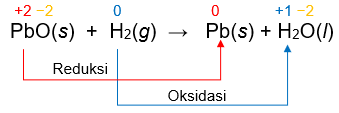
Di antara reaksi-reaksiberikut yang merupakan reaksi redoks adalah ... Ag + ( a q ) + Cl − ( a q ) → AgCl ( s ) CH 3 COOH ( a q ) + NaOH ( a q ) → CH 3 COONa ( a q ) + H 2 O ( l ) Cr 2 O 7 2 − ( a q ) + H 2 O ( l ) → 2 CrO 4 2 − ( a q ) + 2 H + ( a q ) PbO ( s ) + H 2 ( g ) → Pb ( s ) + H 2 O ( l )
Di antara reaksi-reaksi berikut yang merupakan reaksi redoks adalah ...
Jika jawaban (1), (2), dan (3) benar.
Jika jawaban (1) dan (3) yang benar.
Jika jawaban (2) dan (4) yang benar.
Jika hanya jawaban (4) yang benar.
Jika semua jawaban (1), (2), (3), dan (4) benar.
Q. 'Ainillana
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
1
3.9 (12 rating)
Murqiyah Rahmadani Saleh
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Bantu banget Makasih ❤️
yuni nur aini
Jawaban tidak sesuai
Abdullah Salam
Jawaban tidak sesuai
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia