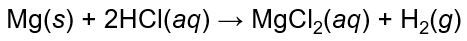Pertanyaan
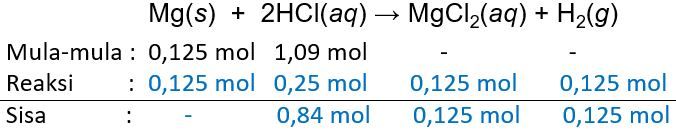
Logam magnesium dengan massa 3 gram direaksikan dengan larutan asam klorida yang mengandung HCl 40 gram. Reaksi yang terjadi adalah: Mg ( s ) + HCl ( a q ) → MgCl 2 ( a q ) + H 2 ( g ) ( belum setara ) Tentukan: a.pereaksi pembatas b. gas hidrogen yang dihasilkan, diukur pada 27°C, 1 atm.
Logam magnesium dengan massa 3 gram direaksikan dengan larutan asam klorida yang mengandung HCl 40 gram. Reaksi yang terjadi adalah:
Tentukan:
a. pereaksi pembatas
b. gas hidrogen yang dihasilkan, diukur pada 27°C, 1 atm.
FH
F. Handiani
Master Teacher
Mahasiswa/Alumni Universitas Negeri Yogyakarta
Jawaban terverifikasi
5
4.8 (10 rating)
LG
Lathifah Gusti Raffri
Mudah dimengerti
A
Adiska
Pembahasan lengkap banget Ini yang aku cari! Mudah dimengerti Makasih ❤️
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia