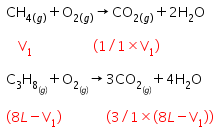Pertanyaan
Pada suhu dan tekanan tertentu, sebanyak 8 liter campuran gas metana dan propana dibakar sehingga dihasilkan20 liter gas CO 2 . Jika diketahui A r C = 12 g mol − 1 , O = 16 g mol − 1 dan H = 1 g mol − 1 , persentase gas metana dan propana dalam campuran tersebut berturut-turut adalah ...
Pada suhu dan tekanan tertentu, sebanyak 8 liter campuran gas metana dan propana dibakar sehingga dihasilkan 20 liter gas . Jika diketahui dan , persentase gas metana dan propana dalam campuran tersebut berturut-turut adalah ...
20% dan 80%
25% dan 75%
40% dan 60%
75% dan 25%
80% dan 20%
YR
Y. Rochmawatie
Master Teacher
Jawaban terverifikasi
12
5.0 (10 rating)
NS
Naudi Sumbersuko
Pembahasannya sesuai😍
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia