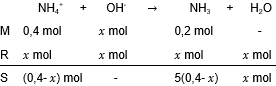Pertanyaan
Suatu larutan penyangga mengandung larutan NH 3 0,2 M ( K b NH 3 = 2 × 1 0 − 5 ) dan NH 4 Br 0,4 M. Jika diinginkan pH larutan bertambah satu satuan, ke dalam 1 L larutan penyangga tersebut harus ditambahkan ...
Suatu larutan penyangga mengandung larutan 0,2 M dan 0,4 M. Jika diinginkan pH larutan bertambah satu satuan, ke dalam 1 L larutan penyangga tersebut harus ditambahkan ...
0, I mol
0,2 mol
0,2 mol
0,3 mol
0,3 mol
AC
A. Chandra
Master Teacher
Mahasiswa/Alumni Universitas Negeri Jakarta
Jawaban terverifikasi
4
3.9 (12 rating)
IK
I Kadek Fredly Sukrata
Makasih ❤️
VM
Viya Minkhatul
Pembahasan lengkap banget
SS
Sylvia Stevanie
Pembahasan tidak lengkap
Pertanyaan serupa
RUANGGURU HQ
Jl. Dr. Saharjo No.161, Manggarai Selatan, Tebet, Kota Jakarta Selatan, Daerah Khusus Ibukota Jakarta 12860
Produk Ruangguru
Bantuan & Panduan
Hubungi Kami
©2026 Ruangguru. All Rights Reserved PT. Ruang Raya Indonesia